Antwort Was befindet sich laut Rutherford in der Atomhülle? Weitere Antworten – Welche Grundbausteine befinden sich laut Rutherford im Kern
Im Atommodell von Rutherford bestehen Atome aus einem massiven Kern aus Protonen und Neutronen und einer Hülle aus Elektronen.Elektrisch ungeladene Atome enthalten in ihrer Hülle genauso viele Elektronen, wie Protonen im Kern. Atome können Elektronen abgeben und werden dann zu elektrisch positiv geladenen Kationen. Atome können Elektronen aufnehmen und werden dann zu elektrisch negativ geladenen Anionen.RUTHERFORD erklärte, dass die ganze Atommasse im Zentrum des Atoms auf einem sehr kleinen Raum vereinigt sei. Dies nannte er den Atomkern.
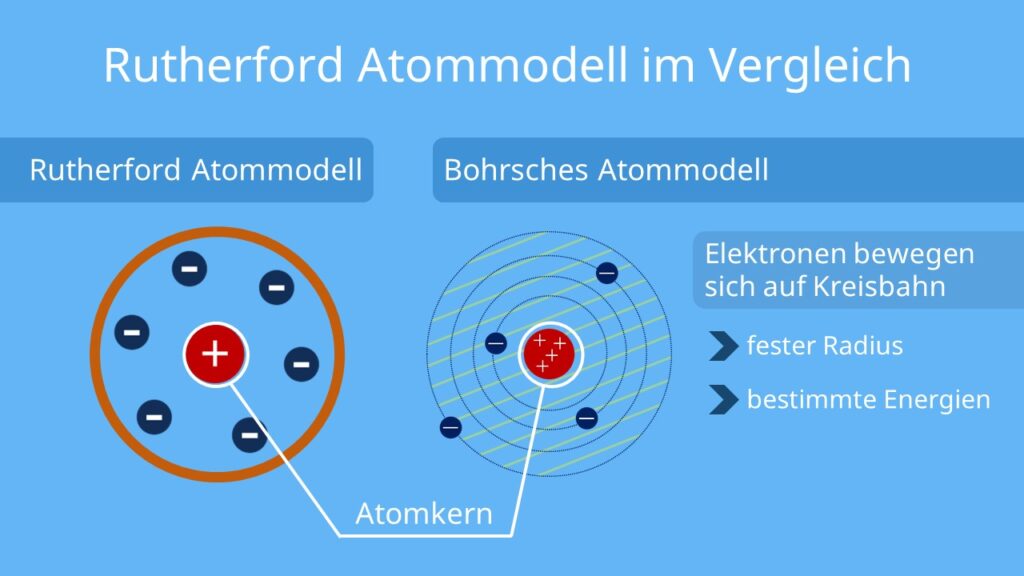
Wie ist ein Atom nach Rutherford aufgebaut : Die wichtigsten Eigenschaften des Rutherford Atommodells sind: Atome bestehen aus einem zentralen Kern und einer Elektronenhülle. Der Kern enthält Protonen und Neutronen. Elektronen sind negativ geladen und umkreisen den Kern.
Welche Schlussfolgerung zog Rutherford aus seinem Versuch
Die einzig logische Schlussfolgerung für Ernest Rutherford war, dass Atome aus einem Kern und einer Hülle bestehen müssen. Im Inneren eines Atoms gibt es das sogenannte Massezentrum, welches positiv geladen ist. Dies nannte er den Atomkern.
Was hat Rutherford entdeckt : Danach war er der Erste, der experimentell nachwies (1919), dass durch Bestrahlung mit Alphateilchen ein Atomkern (in seinem Falle Stickstoff) in einen anderen (in seinem Falle Sauerstoff) umgewandelt werden kann. Bei diesen Experimenten entdeckte er das Proton.
Der Atomkern besteht aus positiv geladenen Protonen und elektrisch neutralen Neutronen. Die Atomhülle besteht aus negativ geladenen Elektronen. In einem Atom entspricht die Anzahl der Elektronen in der Hülle immer der Anzahl der Protonen im Kern.
Das Atommodell nach Rutherford
Der neuseeländische Physiker Ernest Rutherford wollte herausfinden, wo sich diese unterschiedlich geladenen Teilchen innerhalb eines Atoms befinden.
Was hat Rutherford mit dem Streuversuch herausgefunden
Entgegen der Erwartungen wurden sehr wenige Teilchen sogar zurückgestreut! Beim Rutherford Streuversuch konnte auch beobachtet werden, dass die Ablenkung mit hohen Ablenkwinkeln deutlich seltener war. Daher wurden auch nur wenige Alphateilchen genau entgegen der Einstrahlrichtung zurückgestreut.Der Atomkern setzt sich aus positiv geladenen Teilchen, den Protonen sowie den ungeladenen Neutronen zusammen, die wiederum aus anderen Elementarteilchen bestehen. Um den Kern, also in der Hülle, befinden sich die negativ geladenen Elektronen.Mit einem Versuch konnte Rutherford die Annahme der Ladungsverteilung im Atommodell nach Dalton widerlegen. Das Atommodell nach Rutherford geht davon aus, dass Atome aus einem kleinen, massereichen Atomkern bestehen.
Die Atomhülle besteht aus negativ geladenen Elektronen. In einem Atom entspricht die Anzahl der Elektronen in der Hülle immer der Anzahl der Protonen im Kern. Die Ladung, die die geladenen Elementarteilchen (also Elektronen und Protonen) tragen, wird als Elementarladung ( ) bezeichnet und in Coulomb (C) angegeben.
Welche Teilchen befinden sich im Atomkern : Atomkerne bestehen aus Nukleonen. Dies sind entweder die elektrisch positiven Protonen und elektrische neutralen Neutronen. Die Kernladungs- oder Ordnungszahl gibt die Zahl der Protonen in einem Atomkern an und bestimmt, um welches Element es sich handelt.
Was stellte Rutherford fest : Rutherford gilt als einer der bedeutendsten Experimentalphysiker. 1897 erkannte Rutherford, dass die ionisierende Strahlung von Uran aus mehreren Teilchenarten besteht. 1902 stellte er die Hypothese auf, dass chemische Elemente durch radioaktiven Zerfall in Elemente mit niedrigerer Ordnungszahl übergehen.
Was erforschte Rutherford
Rutherford gilt als einer der bedeutendsten Experimentalphysiker. 1897 erkannte Rutherford, dass die ionisierende Strahlung von Uran aus mehreren Teilchenarten besteht. 1902 stellte er die Hypothese auf, dass chemische Elemente durch radioaktiven Zerfall in Elemente mit niedrigerer Ordnungszahl übergehen.
Der Raum zwischen den Orbitalen der Elektronen und dem Atomkern ist erfüllt von virtuellen Photonen und auch einigen wenigen virtuellen Teilchen. Die üblichen Neutrinos beispielsweise durchdringen Kern und Hülle nahezu ohne Wechselwirkung.Ernest Rutherford, 1. Baron Rutherford of Nelson (* 30.
1897 erkannte Rutherford, dass die ionisierende Strahlung von Uran aus mehreren Teilchenarten besteht. 1902 stellte er die Hypothese auf, dass chemische Elemente durch radioaktiven Zerfall in Elemente mit niedrigerer Ordnungszahl übergehen.
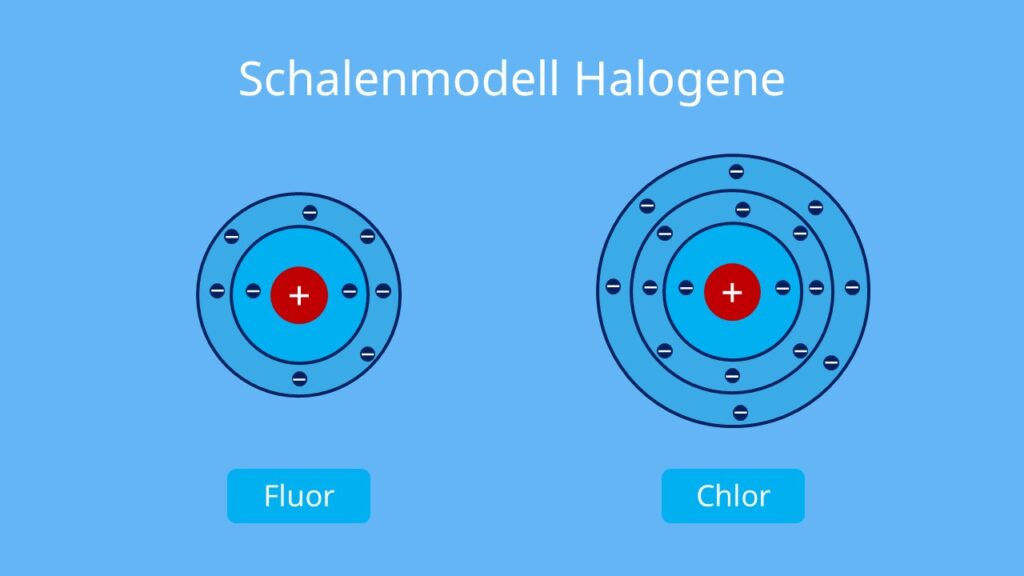
Wie kann man sich die Atomhülle vorstellen : Grob vereinfacht kann man sich die Atomhülle als einzelne ineinanderliegende Schalen vorstellen. In diesen Schalen befindet sich immer eine bestimmte Anzahl an Elektronen.